Lecția 25
Lecția 25 de „săruri“ desigur „Chimie pentru manechine“ învață cum să numesc în mod corect sărurile, compoziția lor și să învețe să facă săruri formule chimice.

După cum sa menționat în acizii lecțiilor anterioare în reacțiile cu H2 hidrogen metalic substanță simplă eliberată. În afară de hidrogen, formată de asemenea substanțe complexe: ZnCl2. . MgSO4 etc. Ei sunt reprezentanți ai clasei comune în chimia compușilor - (. 102 Fig) sare.

Aici ne uităm la compoziția sărurilor, să învețe să facă formulele lor, știu cum să numesc sare.
Sărurile de compoziție
Comparați săruri formula acizi HCl și H2 SO4 c formulele ZnCl2 și FeSO4. Vedem că, în aceste formule sunt anioni identici Cl (I) și SO4 (II). Dar, moleculele de acid sunt conectate la atomii de hidrogen H și sărurile de unități care pot fi definite - cu Zn și Fe atomi de zinc de fier. Prin urmare, acestea și alte săruri pot fi considerate produse de substituție ale atomilor de hidrogen din moleculele acizilor asupra metalelor atomi. Substanțe precum ZnCl2 și FeSO4. aparține unei clase de săruri.
Sărurile - sunt substanțe complexe formate din atomi de metal și reziduuri acide.
Sărurile resturilor acide se leagă la atomii de metal, în conformitate cu valența lor. Pentru prepararea formulei chimice a sării este necesară cunoașterea valența atomului de metal și valența părții de acid. Astfel folosesc aceeași regulă ca și în prepararea compușilor cu formulele binare. Pentru săruri este, de obicei, după cum urmează: suma tuturor unităților valența atomilor de metal trebuie să fie egală cu suma tuturor resturilor de acid unități valența.
De exemplu, formula de sare, care include atomul de calciu și reziduu de acid fosforic al acidului PO4 (III). Calciu prezintă valență constantă II și valența reziduului de acid este PO4 III.

săruri nume
Sărurile formate de atomii de diferite metale și reziduuri acide diferite. Prin urmare, compoziția sărurilor din cele mai diverse. Să învețe să le dea numele corect.
Sărurile Titlu include nume de reziduuri acide și numele metalului în cazul genitiv. De exemplu, compoziția de sare NaCl se numește „clorură de sodiu“.
Dacă o parte a unității formula atomului de metal sare are o valență variabilă, este indicat printr-un număr roman în paranteze după numele său. Astfel, FeCl3 sare numită „clorura de fier (III)» și Sarea FeCl2 - «clorură de fier (II)».
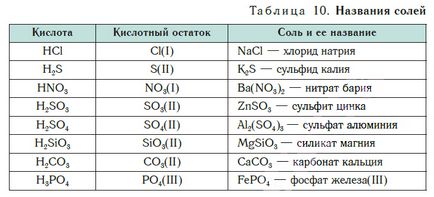
Tabelul 10 prezintă denumirile unor săruri.
Sarea - o structură non-moleculară a materiei. Prin urmare, compoziția sa este exprimată în unități de formulă. Ele reflectă raportul dintre atomii de metal și reziduuri acide. De exemplu, în unitatea formula NaCI per atom de Na au un rest de acid este CI.
Conform formulei chimice a sării poate calcula formula greutatea sa relativă Dl. și M. masa molară De exemplu:
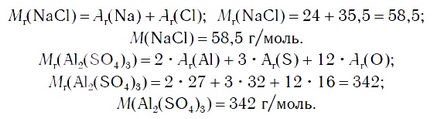
Sărurile nu se referă numai sare (NaCl), dar creta, marmura (CaCO3), carbonat de sodiu (Na2 CO3), permanganat de potasiu (KMnO4), și altele.
Concluzii scurtă lecție:
- Sărurile - substanțe complexe care constau din atomi de metale și anioni.
- Sărurile sunt formate prin substituirea atomilor de hidrogen din moleculele acizilor asupra metalelor atomi.
- Sare - structură non-moleculară a materiei.