analiza enzimatică
Enzimele joaca un rol important în analiza biochimice. In materiale biologice, cum ar fi fluidele corporale, prin determinarea activității catalitice a enzimelor pot fi detectate în concentrații foarte mici. Enzimele pot fi utilizate ca reactivi pentru determinarea concentrațiilor de metaboliți, cum ar fi glucoza din sânge (Schema B). Cele mai multe teste de enzimatice utilizate fotometrie.
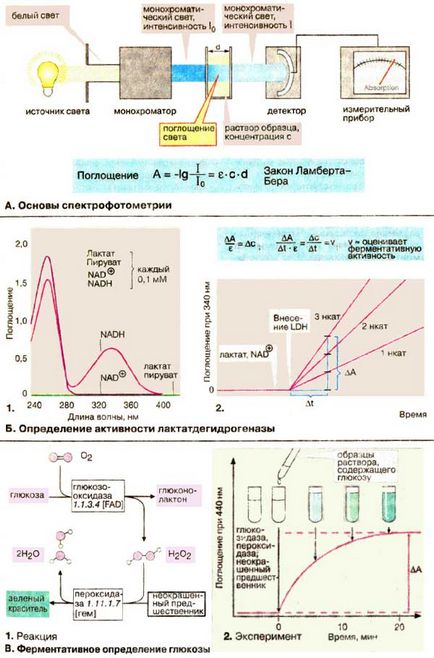
A. Bazele spectrofotometrie
Multe molecule absorb lumina în regiunea vizibilă sau în ultraviolet ale spectrului. Această proprietate poate fi utilizată pentru a determina concentrația. Absorbția depinde de tipul și concentrația substanței, precum și lungimea de undă a luminii folosite. Prin urmare, lumina monocromatică folosit. t. e. lumina unei anumite lungimi de undă care pot fi izolate de lumină albă folosind un monocromator. Intensitatea luminii monocromatică I0 trece prin celula dreptunghiulară din sticlă sau cuarț (cuvă), în care materialul absorbant este o soluție. Intensitatea I a luminii emergente, absorbția alterată este măsurată cu un detector. Absorbția luminii (A) a soluției (densitate optică), determinată ca logaritm negativ al raportul I / I0. Act Lambert-Beer afirmă că A este proporțională cu concentrația (e) substanței și grosimea (d) a stratului de soluție. coeficientul de extincție # 949; depinde, așa cum sa menționat mai sus, tipul de substanță și de lungimea de undă.
B. Determinarea activității lactat dehidrogenazei
Determinarea lactat dehidrogenazei [LDH (LDH)] bazat pe faptul că a redus coenzima NADH + H + absoarbe lumina la 340 nm, în timp ce NAD + (NAD +) la această lungime de undă nu există nici o absorbție. Spectrele de absorbție (m. E. Grafica A în funcție de lungimea de undă) de substrat și coenzima în reacția LDH prezentate în Fig. B1.
Diferențele în absorbția NAD + și NADH între 300 și 400 nm sunt datorate variațiilor inelului nicotinamida în oxidarea sau reducerea (a se vedea. P. 102). Pentru a determina activitatea in cuva a fost plasată în principal soluții de lactat și NAD + și absorbanța este înregistrată la o lungime de undă constantă de 340 nm. reacția necatalitic continuă la o viteză foarte mică. Prin urmare, cantitatea măsurată de NADH formată numai după adăugarea LDH. Deoarece rata de creștere a absorbanței # 916; A / # 916; t pe legea Beer-Lambert este proporțională cu viteza de reacție # 916; c / # 916; t. Activitatea LDH poate fi calculată utilizând un coeficient de extincție # 949; la 340 nm sau prin comparație cu o soluție standard.
Determinarea B. enzimatica glucozei
Cele mai multe biomolecule nu absorb lumina în regiunile vizibile și în ultraviolet ale spectrului. Mai mult, ele sunt de obicei prezente în amestec cu alți compuși care dau, de asemenea, reacții chimice similare. Ambele probleme pot fi depășite printr-o enzimă adecvată pentru conversia selectivă a determinat metabolitul într-o substanță colorată, care a fost determinată în continuare de intensitatea de absorbție a luminii.
Metoda uzuală de determinare a glucozei din sânge (.. 162 cm), se bazează pe două reacții consecutive:
1) formarea de gluconolactonă și peroxid de hidrogen H2 O2 de glucoză oxidazei enzimă;
2) oxidarea unei substanțe incolore de peroxid de hidrogen în compusul de culoare verde într-o reacție catalizată de peroxidaza.
Când toată glucoza disponibilă în eșantion este utilizat în sus, cantitatea de substanțe colorate formate pot fi determinate prin absorbție a luminii, care este direct proporțională cu conținutul inițial de glucoză.